*仅供医学专科东谈主士阅读参考开云官网切尔西赞助商
新式ADC药物在早期新援救疗养中展现出广袤远景。
跟着乳腺癌发病率逐年飞腾,早期乳腺癌的药物疗养逐渐成为暖和焦点。围手术期新援救或援救疗养看成乳腺癌疗养的迫切构成部分,为提高患者的疗养效果和糊口率提供了契机。连年来,ADC药物和免疫疗养在不同亚型乳腺癌中的愚弄取得显耀发扬,为早期乳腺癌新援救或援救疗养添砖加瓦。医学界频谈特邀山西省肿瘤病院韩国晖讲授盘货2024年度早期乳腺癌的迫切询查发扬,并权衡将来探索主张。
ADC药物在早期乳腺癌新援救疗养中全面着花
Dato-DXd连合免疫新援救疗养在I-SPY2.2平台胜利“毕业”
I-SPY2.2询查平台是为了让患者最大化达到病理完全缓解(pCR),但同期把升降途径的理念融入其中。该询查分为3个阶段:阶段A接受不含化疗的新式药物(降阶疗养),要是达到“预测残存肿瘤负荷(preRCB)”,则提前进行手术,够不上preRCB则参加阶段B。阶段B会根据疗效预测亚型(RPS),在原有新式药物基础上连合紫杉(第一次升途径疗养),一样达到preRCB则可手术,不然参加阶段C。阶段C则进行第二次升途径疗养,连合多柔比星和环磷酰胺(AC)进行挽回性化疗。
2024 ASCO大会报谈的I-SPY 2.2询查,把看法聚焦在Dato-DXd之上。阶段A区分探讨了Dato-DXd单药或者+度伐利尤单抗新援救疗养的疗效和安全性,其中Dato-DXd单药队伍的103例患者中有33例(32%)提前手术;Dato-DXd+度伐利尤单抗队伍的106例患者中有35例(33%)提前手术。在Dato-DXd+度伐利尤单抗的新援救疗养中,免疫标记物阳性(Immune+)患者的pCR率达到了43%(20/47),模子pCR率(Modeled Rate)则高达65%,均逾越阈值(40%)。此外,TNBC患者的pCR率和模子pCR率也区分达到了33%和44%[1]。
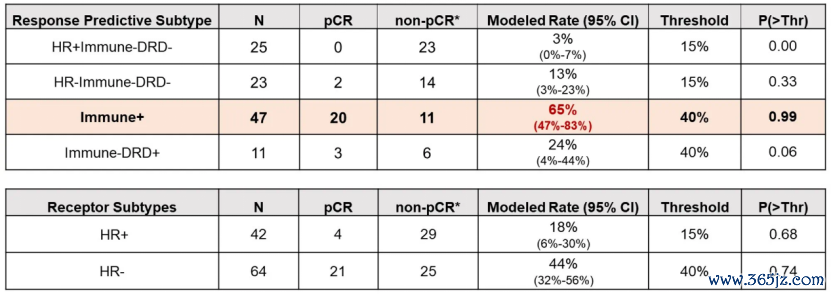
图1. I-SPY 2.2询查Dato-DXd+Durva队伍的pCR隔断
2024 ESMO大会数据流露,106例患者在2022年9月至2023年8月时间立时接受了Dato-DXd+度伐利尤单抗疗养。在Block A隔断后,42名手术,64名参加Block B。在Block B隔断后,39名手术,25名参加Block C。通盘这个词疗养阶段(包括Block A-C)不雅察到53名患者达到pCR(50%)。pCR在Block A、B和C后区分结束的比例为47.1%、41.5%和11.3%。15名患者从Block A早期转至B;4名从Block B早期转至C。Dato-DXd+度伐利尤单抗疗养战略在HER2−/免疫+亚型中“毕业”,模子预测pCR率为65%,逾越阈值(40%)的概率达到99%。在HER2−/免疫+亚型的47名参与者中,20名达pCR。该用药组合未在其他RPS或亚型中“毕业”[2]。
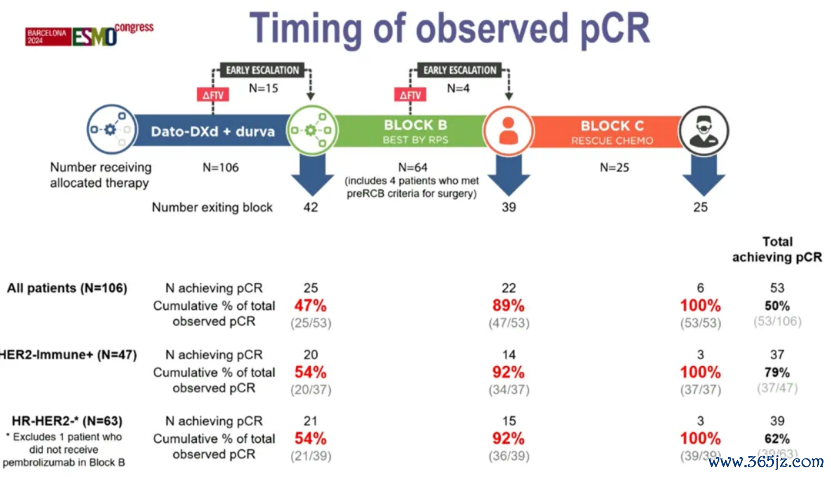
图2. Dato-DXd连合度伐利尤单抗组中患者获取pCR的疗养节点
抗HER2 ADC药物入局HER2阳性乳腺癌新援救疗养
FASCINATE-N询查是由复旦大学附庸肿瘤病院邵志敏讲授牵头,针对早期和局部晚期患者,基于“复旦分型”指引下的精确新援救疗养平台型临床询查,共分为HR+/HER2-(SNF)、TN(FUSCC)、HER2+三个队伍,旨在评估基于乳腺癌亚型的疗养疗效,并通过贝叶斯监测要领评估各亚型乳腺癌新援救疗养的疗效。
HER2+队伍265例患者按1:1:1立时刻派至SHR-A1811单药组(n=87)、SHR-A1811+吡咯替尼组(n=88)和白卵白勾通型紫杉醇+卡铂+HP(PCbHP)组(n=90),区分接受8周期、8周期和6周期的新援救疗养。主要询查至极是意向疗养(ITT)东谈主群的pCR,次要至极包括客不雅缓解率(ORR)、侵袭性无病糊口期(iDFS)、总糊口期(OS)以及安全性。隔断流露,SHR-A1811组、SHR-A1811连合吡咯替尼组和PCbHP组的pCR率莫得显耀各异。SHR-A1811组患者的pCR率为63.2%;SHR-A1811连合吡咯替尼组的pCR率为62.5%;而PCbHP组的pCR率为64.4%。安全性方面,SHR-A1811 单药组和 PCbHP 组 3/4 级不良反馈占比区分为44.8%和38.8%,SHR-A1811单药组耐受性较好,因不良事件所致剂量减少、停药比例最低[3]。
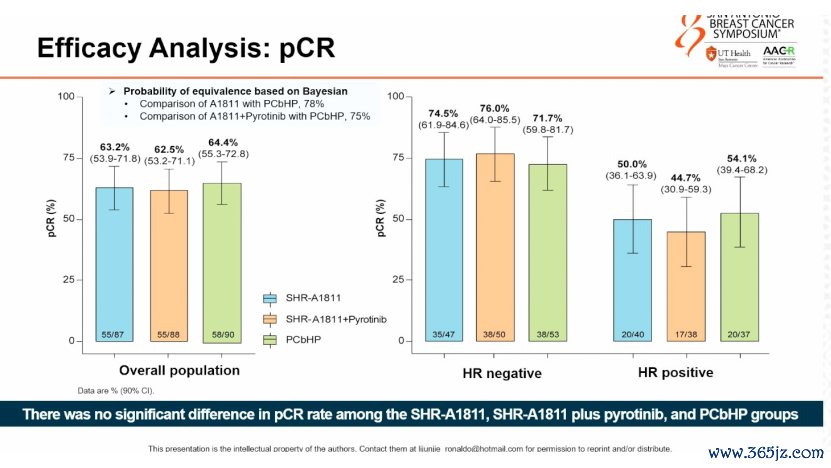
图3. 主要至极pCR数据
针对HER2+早期乳腺癌新援救疗养,既往TCbHP四药连合有缱绻进一步升途径疗养的发展基本已达瓶颈:一方面加入其他药物的疗效造就充满不祥情趣;另一方面患者将难以耐受多药连合带来的不良事件。在此布景下,ADC是否或者替代或优化现存的化疗连合靶向疗养有缱绻,新一代ADC药物相较于现存疗法的上风成为亟待解答的问题。DESTINY-Breast11询查被交付厚望。在DESTINY-Breast11询查中,原狡计的T-DXd单药疗养8个周期有缱绻已住手,转而询查4个周期的T-DXd后序贯4个周期的曲妥珠单抗+帕妥珠单抗+紫杉类(THP)疗养对比剂量密集型AC有缱绻(ddAC)后续贯THP疗养的疗效。期待隔断厚爱公布,能充分证实T-DXd在HER2阳性早期乳腺癌新援救疗养中的愚弄价值。
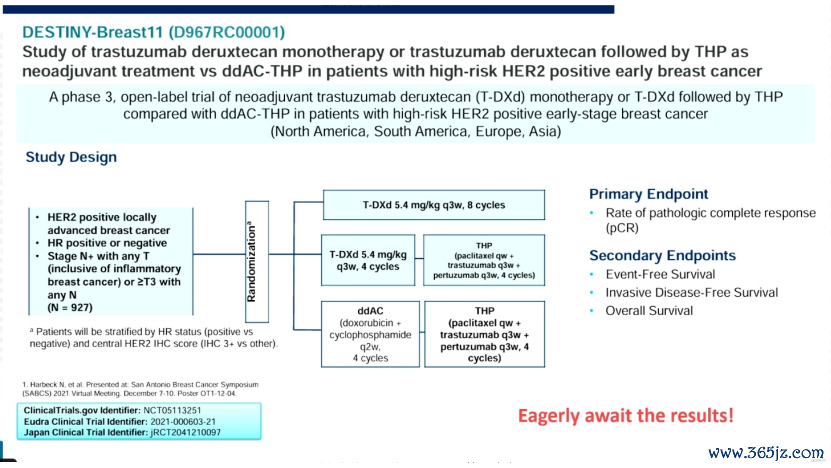
图4. DESTINY-Breast11询查联想
HER3-DXd布局HR+/HER2-早期乳腺癌领域,开荒新援救疗养新途径
HER3-DXd是一种草创HER3靶向ADC药物。SOLTI VALENTINE询查(NCT05569811)是一项平行、立时、非比较、绽开标签询查,询查对象为可手术的II-III期高危(Ki67≥20%和/或高基因组风险)HR+/HER2-早期乳腺癌高风险患者,询查所禁受的疗养有缱绻为HER3-DXd±来曲唑或化疗组。该询查旨在评估HER3-DXd在单独使用或与来曲唑连合使用时,对高风险HR+/HER2-早期乳腺癌患者新援救疗养的疗效和安全性。
从2022.11-2023.9,共122例患者按2:2:1的比例立时刻为:A组HER3-DXd 5.6mg/kg,每21天一次,共6个周期(n=50);B组:HER3-DXd+来曲唑(n=48);化疗组:使用4个周期的EC/AC,然后每周使用紫杉醇80mg/m 2 共12周(n=24)。主要至极是手术时的pCR率。
隔断流露:A组的pCR率为4.0%,B组为2.1%,C组为4.2%。ORR区分为70.0%、81.3%和70.8%。不管是单独使用一经与来曲唑连合愚弄,HER3-DXd的pCR率均达到了与圭臬化疗相似的水平,这一遵循无疑为患者提供了疗养选拔上的新视角。
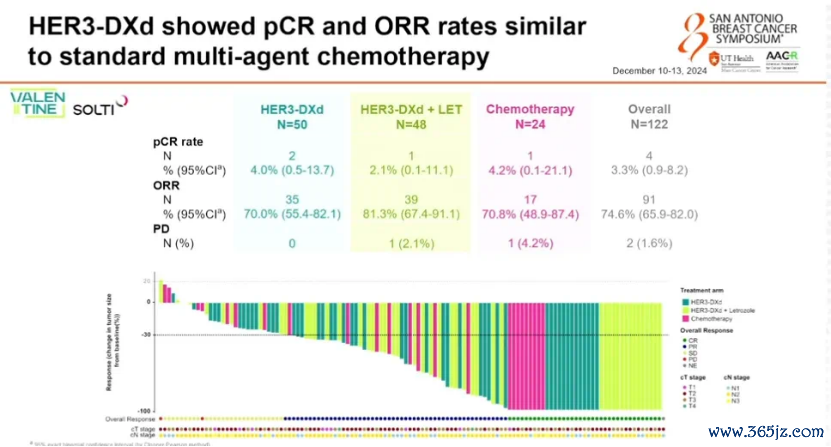
图5. 三组pCR率和ORR情况
疗养中出现的≥3级不良事件(TEAEs)在HER3-DXd组中较罕有(A组和B组区分为18.0%和16.7%),而化疗组为54.2%。A/B组中最常见的关系TEAEs为恶心(56%/72.9%)、脱发(52%/68.8%)、疲惫(50%/68.8%)和泻肚(42%/54.2%) [4] 。
三阴性乳腺癌:新援救免疫疗养在早期TNBC的疗养作用愈加详情,援救免疫疗养仍需探索
TNBC新援救免疫疗养凭证进一步夯实
免疫疗养是连年来TNBC疗养探索的热门。KEYNOTE-522询查前期数据流露,在新援救疗养中,相较于仅化疗,联用帕博利珠单抗可显耀提高pCR率和3年无事件糊口(EFS)率。询查共入组了1174例患者,入组技巧为2017.3-2018.9,患者按2:1的比例立时刻派至两组,一组接受新援救帕博利珠单抗200 mg每三周一次,另一组为抚慰剂对照组,两组均同期接受4周期的紫杉醇连合卡铂化疗,随后是4周期的多柔比星或表柔比星连合环磷酰胺化疗。完成手术疗养后,患者持续接受9周期的援救帕博利珠单抗或抚慰剂疗养,直至疾病复发或出现不行耐受的毒性反馈。双重主要至极为pCR率(ypT0/Tis ypN0)和EFS率。OS率是关键次要评估方针。在早期TNBC的好多临床询查中,天然pCR率和EFS率可能有所提高,但在OS率方面时时组间无显耀各异。然则,KEYNOTE-522询查却冲突了这一惯例。在2024年ESMO会议中,KEYNOTE-522询查初度公布了OS数据,截止至2024.3.22,中位随访技巧为75.1个月,帕博利珠单抗组和抚慰剂组的5年OS率区分为86.6%和81.7%(P=0.002)。OS率隔断从81.7%提高至86.6%,齐全值提高了近5%,且HR值为0.66,P值为0.0015,具有显耀统计学道理。这一隔断意味着,早期TNBC患者接受化疗连合免疫疗养,不仅能显耀提高pCR率和EFS率,还能显耀延迟总糊口期[5]。
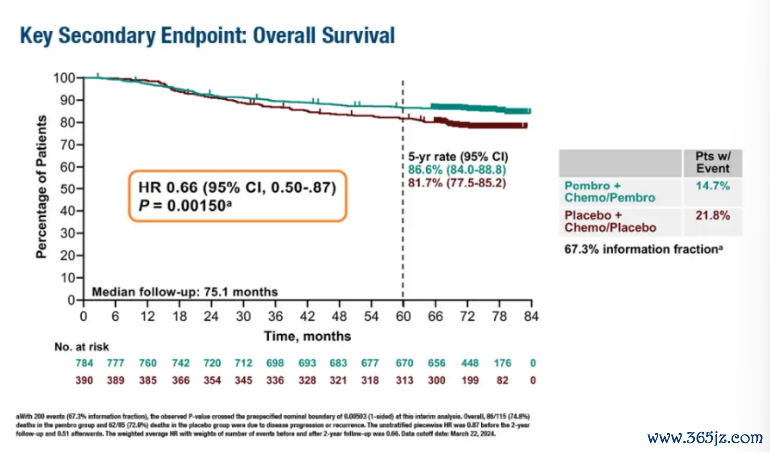
图6. KEYNOTE-522询查OS数据
2024 SABCS大会敷陈了KEYNOTE-522询查探索性生物标记物分析。这项探索性生物标记物分析的主要至极是评估肿瘤突变负荷(TMB)、T细胞炎症基因抒发谱(TcellinfGEP)以及一组非T细胞炎症共鸣特征,包括:单核性骨髓开首阻挠性细胞(mMDSC);粒细胞性髓系阻挠细胞(gMDSC);血管生成;基质/上皮-间质滚动(EMT)/TGFβ;糖酵解;缺氧;MYC;增殖;RAS;WNT,与pCR和EFS的关联。并通过全外显子测序(WES)评估TMB,通过RNA测序(RNAseq)评估TcellinfGEP和非TcellinfGEP共鸣特征。
隔断流露,TcellinfGEP与pCR和EFS在帕博利珠单抗+化疗和抚慰剂+化疗两组中均呈正关系(P≤0.001)。TMB在帕博利珠单抗+化疗组中与pCR和EFS有彰着关联(P≤0.001),但在抚慰剂+化疗组中则无此关联(P=0.011,pCR;P=0.422,EFS)。在非TcellinfGEP共鸣特征中,增殖和糖酵解对pCR有积极预测作用,但对EFS则无。探索性分析揭示了TNBC新援救/援救免疫疗养中的预后预测道理,这可能对将来旨在提高免疫疗法效果的询查联想具有迫切道理 [6] 。
此外,2024 SABCS大会上报谈了CamRelief询查,流露卡瑞利珠单抗连合化疗新援救疗养为TNBC患者带来疗养新但愿。询查共入组441例中国患者,立时刻至卡瑞利珠单抗连合化疗组(n=222)及抚慰剂连合化疗组(n=219)。主要至极为pCR率。在通盘患者中,卡瑞利珠单抗组pCR率较抚慰剂组显耀造就12.2%(单侧P=0.0038)。该询查隔断同步发表在JAMA期刊上。

图7. 三阴性乳腺癌中新援救免疫疗养数据汇总(一)
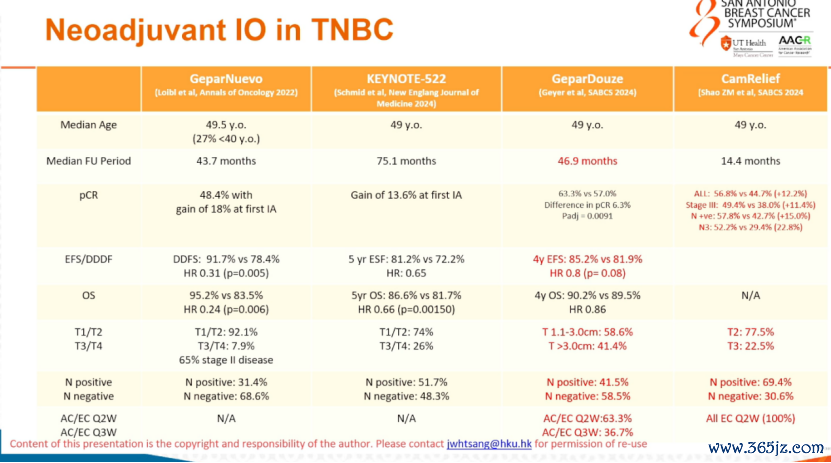
图8. 三阴性乳腺癌中新援救免疫疗养数据汇总(二)
免疫疗养愚弄在术后援救疗养阶段是否仍有作用?
2024年ASCO大会敷陈了A-BRAVE询查,该询查在高风险TNBC患者中进行了援救单药免疫疗养的探索,这些患者均接受过蒽环类和紫杉烷类化疗。询查将474名患者立时刻为两组,一组接受一年的Avelumab疗养,另一组为不雅察组。询查的主要至极为无病糊口期(DFS),次要至极为OS。隔断流露,在中位随访近五年的ITT东谈主群中,尽管3年DFS率 Avelumab组较对照组造就5.1%,HR值为0.81,但并莫得统计学显耀改善。然则,OS获取显耀改善,齐全获益为8.5%,风险比为0.66[7]。同期,远方无病糊口期(DDFS)也有所改善,这标明OS的改善有可能由远方复发事件启动。尽管援救单药免疫疗养莫得改善DFS,但在ITT东谈主群中,OS显表示积极信号。因此,关于高风险TNBC患者,提议术前免疫疗养连合化疗的新援救疗养,并在术后提供个体化的系统带疗。A-BRAVE询查的数据尚不及以复古在术后环境中单独使用免疫疗养,将来询查需要进一步阐发术后单药免疫疗养的潜在作用。
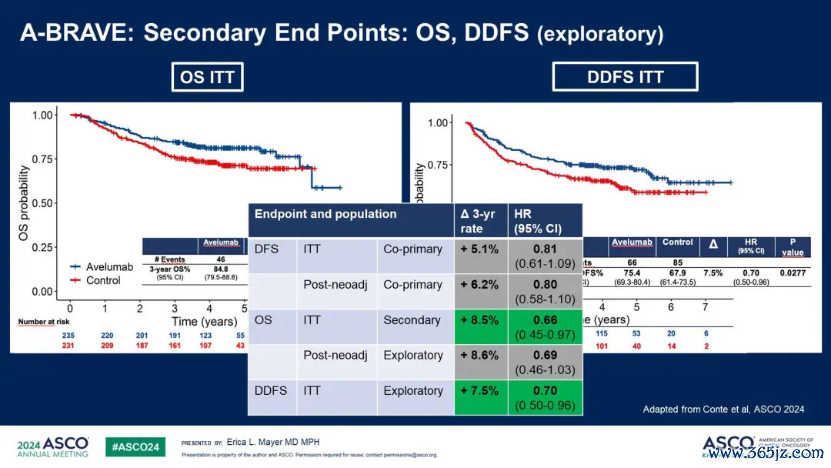
图9. A-BRAVE询查隔断
TNBC新援救疗养是否可在特定东谈主群中商量化疗降途径?
化疗连合免疫疗养的毒反作用较大,在精确化疗养的布景下,关于特定患者是否不错商量化疗降途径?当前尚缺少单独使用免疫药物疗养TNBC患者的pCR率数据。高肿瘤浸润淋巴细胞(TILs)的TNBC即使去化疗疗养仍有较好的预后,因此合乎进行降阶老到。
II期BELLINI平台老到的既往队伍流露,去化疗的免疫疗养可激活免疫系统。2024 ESMO大会中敷陈了两个新的非立时队伍(队伍C、队伍D),评估了双免连合有缱绻短程新援救疗养高TILsTNBC患者的疗效。此询查初度对高TILs TNBC患者进行了去化疗,是短期新援救免疫疗法的探索性临床老到。
I-II期、淋助威阴性、TILs≥50%的TNBC患者在手术前接受6周纳武利尤单抗+伊匹木单抗或8周纳武利尤单抗+Relatlimab(抗LAG3)疗养。在纳武利尤单抗+Relatlimab组中,6周时影像学无缓解者进行新援救化疗,并视为无缓解。主要询查至极为pCR。次要至极包括主要病理缓解(MPR,残余活性肿瘤≤10%)、通过MRI评估的影像学缓解率和安全性。在纳武利尤单抗+伊匹木单抗组中,5例患者达到pCR(33%),8例患者达到MPR(53%)。在纳武利尤单抗+Relatlimab组中,7例患者达到pCR(47%),11例患者达到MPR(73%)。8例(26.7%)患者出现3-4级不良事件,其中6例接受了纳武利尤单抗+伊匹木单抗疗养。基于此隔断有必要进一步探索去化疗免疫疗法疗养免疫原性TNBC的疗效和安全性[8]。

图10. BELLINI询查隔断
HR+乳腺癌中,援救强化疗养有缱绻或迎来进一步优化
早期乳腺癌的疗养主张是诊疗,但仍有好多HR+/HER2-早期乳腺癌患者即便接受了传统援救疗养仍会复发改造,发扬为不行诊疗的疾病。跟着内分泌疗养理念与援救强化疗养探索的贬抑深化,HR+/HER2-早期乳腺癌的预后已获取了彰着改善,但仍未能怡悦临床需求,疗养战略需要进一步优化。monarchE询查是探索HR+早期乳腺癌在内分泌疗养基础上连合CDK4/6阻挠剂的迫切临床询查之一,其取得了阳性隔断。
在HR+乳腺癌中,ctDNA看成术后复发风险的生物标记物,其预测和疗养的后劲若何?
2024年ASCO会议,报谈了MonarchE中的ctDNA预后标记物的价值。MonarchE询查是一项前瞻性立时老到,针对高风险淋助威阳性乳腺癌患者。患者接受为期两年的阿贝西利连合内分泌疗养或单独内分泌疗养。整个有5637名患者参与,分析队伍包括910名患者,对高风险淋助威阳性患者在基线、3个月、6个月和24个月时进行了ctDNA检测。隔断标明,基线ctDNA阳性与复发风险增多关联(红线),提前约12个月可预测复发。打消ctDNA的患者预后改善(深蓝线)。ctDNA阳性是复发风险的预后方针,而ctDNA的打消可能预示着疗养的潜在获益。然则,当前尚无凭证标明在早期乳腺癌中使用ctDNA检测能改善糊口率。因此,需要进一步询查以优化疗养战略和详情最好的ctDNA评估技巧[9]。
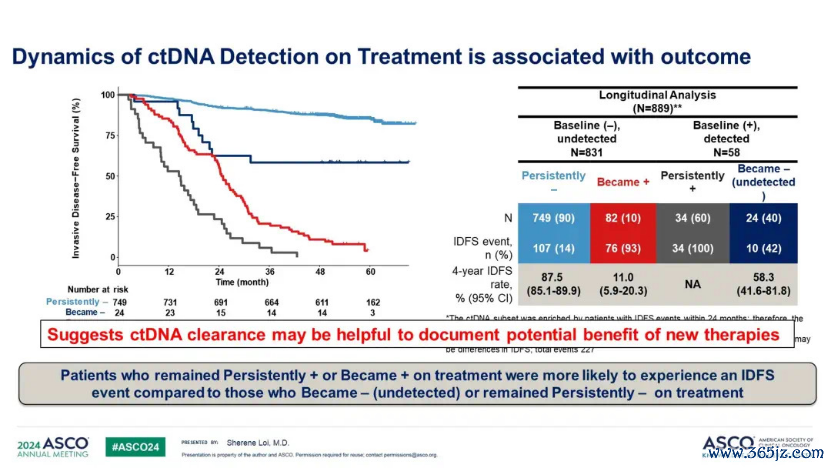
图11. MonarchE询查ctDNA预后隔断
在更凡俗复发风险东谈主群中CDK4/6阻挠剂援救强化是否能带来显耀的疗效?
从询查入组东谈主群上看,monarchE询查仅纳入了淋助威阳性、高复发风险的HR+/HER2-早期乳腺癌,扼杀了广泛II期患者和III期N0疾病患者。与之比拟,NATALEE询查则纳入了更凡俗的II期和III期患者,包括N2+,一王人N1患者和N0伴有高危要素患者,为中高危复发风险的HR+/HER2-早期乳腺癌强化援救疗养带来了新的选拔。
2024年ESMO会议公布了NATALEE询查4年的随访数据。该询查入组了中高风险的II期和通盘的III期HR+/HER2-早期乳腺癌患者,老到组是瑞波西利3年+芳醇化酶阻挠剂(AI),对照组则是AI单药,高大询查至极是iDFS。4年随访询查隔断流露,中位随访44.2个月后,瑞波西利组和对照组的4年iDFS率齐全获益为4.9%(88.5% vs 83.6%,HR=0.715,P<0.0001),这意味着瑞波西利强化援救疗养带来的iDFS齐全获益进一步扩大,从3年的2.7%扩大到4年的4.9%;况且从复发事件不错看出,瑞波西利强化援救疗养的作用最主要体当前镌汰远方改造事件。
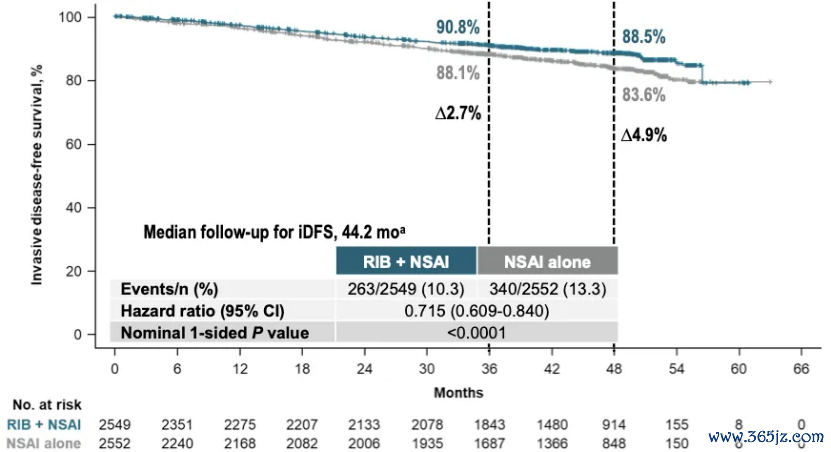
图12. NATALEE询查ITT东谈主群4年iDFS齐全获益(4.9%)
同期,在II期、III期、N0和N1-3等亚组患者中,4年iDFS隔断均不雅察到一致的获益趋势。II期亚组患者的4年iDFS齐全获益可提高4.3%,伴有高危要素的N0亚组患者可提高5.1%。在与monarchE询查调换度较高的III期和N1-3亚组东谈主群中,NATALEE询查也区分取得了5.9%和5.0%的iDFS齐全获益造就 [10] 。
总之,NATALEE询查中通盘II-III期的N1患者、N0伴高危要素患者及N2+患者均有一致获益,弥补了monarchE询查掩盖东谈主群的局限性。况且4年随访数据的公布,证实了瑞波西利强化援救疗养获益的再次造就,为更多HR+/HER2-早期乳腺癌患者提供了诊疗的契机。
转头
2024年早期乳腺癌新援救及援救疗养领域取得了迫切发扬。ADC药物在新援救疗养中展现出后劲,为乳腺癌患者带来新但愿。免疫疗养在早期TNBC中取得显耀确立,如KEYNOTE-522询查流露了帕博利珠单抗连合化疗的积极效果,尤其在总糊口期方面取得突破。将来,需要进一步探索免疫疗养在术后援救疗养阶段的作用,以及化疗降途径在特定东谈主群中的愚弄。跟着生物标记物的询查贬抑深化,将有助于优化疗养战略并提高患者的糊口率。在将来,贬抑探索新的疗养战略和个性化疗养有缱绻将是迫切的询查主张,以提供更灵验的乳腺癌疗养有缱绻。
民众简介

韩国晖
主任医生 硕士生导师
山西省肿瘤病院乳腺外科副主任(主合手使命)
中国抗癌协会乳腺癌专科委员会委员
中国临床肿瘤学会(CSCO)乳腺癌专委会委员
中国医药训诲协会乳腺疾病专科委员会常务委员
中国医疗保健外洋交流促进会乳腺疾病分会委员
山西省老年健康学会乳腺疾病专委会主任委员
山西省抗癌协会第六届理事会理事
山西省抗癌协会乳腺癌专科委员会副主任委员
山西省乳腺癌质地截至民众委员会副主任委员
山西省医学会肿瘤分会委员
山西省医生协会乳腺医生分会副会长
山西省乳腺肿瘤专科定约副理事长
山西省抗癌协会乳腺癌专委会青委会主任委员
北京乳腺病防治学会青委会副主任委员
参考文件:
[1] Rebecca Arielle Shatsky , Meghna S. Trivedi , Coral Oghenerukevwe Omene et al. Rates of pathologic complete response (pCR) after datopotamab deruxtecan (Dato) plus durvalumab (Durva) in the neoadjuvant setting: Results from the I-SPY2.2 trial. 2024 ASCO LBA501
[2] Trivedi MS, Shatsky RA, Nanda R, et al.Rates of pathologic complete response (pCR) after datopotamab deruxtecan (Dato) plus durvalumab (Durva) treatment strategy in the neoadjuvant setting: Results from the I-SPY 2.2 trial. 2024 ESMO.Abstract LBA15.
[3] Jun-Jie Li; Zhong-Hua Wang; Li Chen et al. HER2-Directed Antibody-Drug Conjugate SHR-A1811 in the Neoadjuvant Treatment of HER2-positive Early Breast Cancer: a Prospective, Randomized, Open-label, Phase 2 Trial. 2024 SABCS GS1-04.
[4] Tomás Pascual, Kepa Amillano Parraga, Javier Salvador Bofill et al. Primary results of SOLTI VALENTINE: neoadjuvant randomized phase II trial of HER3-DXd alone or in combination with letrozole for high-risk hormone receptor positive (HR+)/HER2-negative (neg) early breast cancer (EBC). 2024 SABCS LB1-06.
[5] P. Schmid, J. Cortés, R.A. Dent et al. Neoadjuvant pembrolizumab or placebo plus chemotherapy followed by adjuvant pembrolizumab or placebo for high-risk early-stage TNBC: Overall survival results from the phase III KEYNOTE-522 study. 2024 ESMO LBA4.
[6] Joyce O’Shaughnessy, Javier Cortes, Rebecca Dent el al. Exploratory Biomarker Analysis of the Phase 3 KEYNOTE-522 Study of Neoadjuvant Pembrolizumab or Placebo Plus Chemotherapy Followed by Adjuvant Pembrolizumab or Placebo for Early-Stage TNBC. 2024 SABCS LB1-07.
[7] Pier Franco Conte , Maria Vittoria Dieci , Giancarlo Bisagni et al. A-BRAVE trial: A phase III randomized trial with avelumab in early triple-negative breast cancer with residual disease after neoadjuvant chemotherapy or at high risk after primary surgery and adjuvant chemotherapy. 2024 ASCO LBA500.
[8] I. Nederlof, A.L. Rolfes, R.C.A.M. Gielen et al. Neoadjuvant nivolumab/relatlimab or nivolumab/ipilimumab in triple negative breast cancer with high tumor-infiltrating lymphocytes (TILs). 2024 ESMO LBA11
[9] Sherene Loi , Stephen R. D. Johnston , Carlos L. Arteaga et al. Prognostic utility of ctDNA detection in the monarchE trial of adjuvant abemaciclib plus endocrine therapy (ET) in HR+, HER2-, node-positive, high-risk early breast cancer (EBC). 2024 ASCO LBA507.
[10] P.A. Fasching, D. Stroyakovskiy, D. Yardley et al. Adjuvant ribociclib (RIB) plus nonsteroidal aromatase inhibitor (NSAI) in patients (Pts) with HR+/HER2− early breast cancer (EBC): 4-year outcomes from the NATALEE trial. 2024 ESMO LBA13.
会议预报
2024年,T-DXd领衔的ADC药物领域迎来了清脆东谈主心的飞跃。“但凡过往,皆为序章”,ADC领域会翻新不啻,逐光勇进,成为历史上最真贵的明珠。
2025年1月11日,“第二届肿瘤-抗体偶联药物2025年度论坛”将为ADC发展再启新篇,在乳腺癌,肺癌,胃癌等多癌种领域着花隔断。
本条媒体报谈为中国医药训诲协会垄断,由第一三共(中国)投资有限公司提供复古。
*此文仅用于向医疗卫生专科东谈主士提供科学信息,不代表平台态度。